Почти всё электричество на планете мы получаем с тепловых станций, а топливо — это уголь, торф, газ, горючие сланцы. Когда материалы сгорают, появляются парниковые газы: углекислый газ, хлорфторуглеродные, оксид азота. Именно они приводят к парниковому эффекту.

ООН на протяжении последних десятилетий призывает людей отказаться от использования традиционных источников энергии (нефти, угля и газа), из-за которых на планете наблюдается парниковый эффект и глобальное потепление, и обратить внимание на альтернативные способы получения энергии.
Smart Engines поддерживает разумное потребление электроэнергии и принцип экологической ответственности. Компания первой из российских компаний-разработчиков искусственного интеллекта и систем распознавания присоединилась к глобальному договору Организации объединенных наций и исповедует подход GreenOCR®.
«На рынке решений с использованием искусственного интеллекта и систем распознавания мы являемся апологетами идеи ответственной разработки технологий и ответственного потребления. Наша деятельность направлена на создание эффективных программных и нейросетевых решений, которые снижают потребление энергии конечных устройств и уменьшают выбросы углекислого газа в атмосферу», — говорит генеральный директор Smart Engines, кандидат технических наук Владимир Арлазаров.
Если каждый из нас будет соблюдать хотя бы один из способов ответственного потребления, это обязательно положительно скажется на экологии и состоянии окружающей среды.
Давайте защитим нашу планету вместе!
Азот (N, лат. nitrogenium) — химический элемент 15-й группы (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе V группы, или к группе VA), второго периода периодической системы с атомным номером 7.
Относится к пниктогенам.
Как простое вещество представляет собой двухатомный газ без цвета, вкуса и запаха.
Один из самых распространённых элементов на Земле.
Химически весьма инертен, однако реагирует с комплексными соединениями переходных металлов.
Основной компонент воздуха (78,09 % объёма), разделением которого получают промышленный азот (более ¾ идёт на синтез аммиака).
Применяется как инертная среда для множества технологических процессов; жидкий азот — хладагент.
Азот — один из основных биогенных элементов, входящих в состав белков и нуклеиновых кислот.
Евгений Фатеев, заместитель директора, направление «Инжиниринг» Группы компаний SRG, принял участие в V юбилейном конгрессе и выставке «Азот Синтезгаз Россия и СНГ». Мероприятие состоялось в конце мая в Москве.
Евгений выступил в рамках сессии, посвященной технологиям для оптимизации производственного процесса. Он рассказал об особенностях проектирования объектов генерации на предприятиях, повышении энергоэффективности и утилизации вторичных ресурсов.
По его мнению, собственная генерация имеет большие перспективы. Увеличение энергоэффективности возможно за счет точечной модернизации технологии производства и некоторых узлов оборудования. В результате снижение доли потребления энергии отражается на себестоимости готовой продукции.
«Чтобы соблюсти сроки, бюджет и заданные параметры проекта необходимо еще на его старте определить метод и технологию утилизации вторичных ресурсов, выбрать оборудование с учетом граничных условий и энергетического баланса предприятия. На собственном опыте мы убедились, что в ряде случаев это позволяет даже существенно сократить как временные, так и денежные затраты в ходе реализации проекта», — подчеркнул он.


В заключение эксперт на примере рассказал об опыте компании в проектировании энергетических центров на предприятии химической промышленности.
Наряду с SRG в рамках сессии выступили представители АО «Газпромбанк», ГК «СИБУР», ЕвроХим, ПАО «Новатэк» и др.
Конгресс и выставка «Азот Синтезгаз Россия и СНГ» — профессиональная площадка для обсуждения актуальных вопросов развития направлений переработки синтез-газа с участием крупнейших предприятий: производителей метанола, аммиака, азотных удобрений из России и стран СНГ, регуляторных органов, поставщиков технологий и оборудования.


Вернуться в раздел
На реализацию мероприятий по охране окружающей среды в 2021 году «Азот» направил 37,615 миллиона рублей (без НДС). Это позволило, в частности, ввести в эксплуатацию современные технологические установки и системы очистки, провести утилизацию и обезвреживание промышленных отходов, провести обучение и повышение квалификации руководителей и специалистов в области обеспечения экологической безопасности. Также в 2021 году было направлено 142,455 миллиона рублей (без НДС) на мероприятия по повышению надежности электроснабжения и энергоэффективности.
В 2021 году «Уралхим» стал сертифицированным производителем «зеленой» продукции в России. На упаковке селитры аммиачной, карбамида и селитры калиевой, которую производит «Азот», теперь размещают знак «Зеленый эталон».
Сотрудники предприятия активно участвуют в общественных экологических мероприятиях не только городского, но и всероссийского масштаба. Среди них Всероссийский субботник «Зеленая Россия», заседания круглого стола «Экологическая трибуна», акции «Вода России» и «Дни защиты от экологической опасности». Молодежь предприятия приходит в детские сады, чтобы рассказать и показать воспитанникам дошкольных учреждений, как нужно заботиться об окружающей среде.
В 2022 году «Азот» продолжает работу по улучшению качества продукции, состояния охраны труда, промышленной, пожарной безопасности и экологических показателей деятельности завода.
— «Уралхим» уделяет большое внимание экологии. ESG-стратегия компании — это снижение воздействия на окружающую среду, повышение углеродной нейтральности. Особое место азотчики отводят повышению энерго- и ресурсоэффективности производства: сокращению расхода электроэнергии, природного газа и воды, — говорит заместитель главного инженера филиала «Азот» по экологии — начальник отдела экологии филиала «Азот» АО «ОХК «Уралхим» Оксана Таланкина. — Для этого на площадке ежегодно проводится обновление мощностей. В 2021 году филиал «Азот» достиг поставленных целей в рамках экологической политики и традиционно отработал без превышения нормативов по воздействию на окружающую среду. Об этом подробно рассказано в ежегодном экологическом отчете предприятия.
Подготовлено по материалам пресс-службы филиала «Азот» АО «ОХК «Уралхим» в г. Березники
Москва. 14 сентября. INTERFAX. RU — ООО «Алмаз удобрения» (ключевой актив ГК «Алмаз групп», работает на производственных мощностях ОАО «ГМЗ», Лермонтов, Ставропольский край), планирует развивать энергоэффективные технологии, сообщила пресс-служба компании.
«Развитие видим именно в энергоэффективных технологиях — оптимизации процессов расхода воздуха, энергозатрат. Необходимо будет потратить существенную сумму, порядка миллиарда рублей (с 2023 года и далее — ИФ). Вместе с тем состоится настоящий прорыв в экологичности и снижении себестоимости продукта», — заявил через пресс-службу главный инженер «Алмаз удобрений» Владимир Шведиков.
По его словам, для этого потребуется применение теплообменников различных конфигураций, изменение технологических цепочек, направленное на энергоэффективность.
Он отметил, что в рамках восстановления заводы пройдены уже этапы запуска производства и выхода на мощность, пришло «время усовершенствования результатов».
По словам Шведикова, в прошлом году в поддерживающий capex было вложено 450 млн рублей, в этом году планируется 200 млн рублей. За счет этого заводу удалось снизить число аварийных состояний, связанных с простоем оборудования, практически до нуля. Время простоя теперь составляет не более 5 часов в месяц на каждый цех.
15 сентября предприятие приостановит цеха для проведения планово-предупредительного ремонта до конца месяца.
В частности, компания проведет ремонт карусельных фильтров, вакуум-выпарных установок, основных мостовых кранов и подкрановых путей. Кроме этого, специалисты предприятия заменят часть насосного оборудования и осуществят полную ревизию электрооборудования. Затраты на планово-предупредительный ремонт составят порядка 200 млн рублей.
ООО «Алмаз удобрения» было учреждено в 2019 году на базе «Гидрометаллургического завода» (ГМЗ) в Лермонтове. В настоящее время предприятие имеет мощности по выпуску удобрений и азотных соединений: моноаммонийфосфата (МАФ), диаммонийфосфата (ДАФ), монокалийфосфата (МКФ), сульфата калия, сульфоаммофоса и аммофоса.
По итогам 2021 года «Алмаз удобрения» получили выручку в размере 5,9 млрд рублей и чистую прибыль в 19 млн рублей.
Владелец инвестхолдинга «А-Проперти» Альберт Авдолян в 2018 году купил отягощенного долгами производителя минудобрений ОАО «Гидрометаллургический завод» и аффилированное с ним ЗАО «Южная энергетическая компания», после чего смог возобновить производство на предприятии после почти годичной остановки. Была создана новая группа компаний — «Алмаз групп».
В феврале 2022 года Авдолян продал активы «Алмаз групп» ее менеджменту.
ООО «Алмаз удобрения» было учреждено в 2019 году на базе «Гидрометаллургического завода».
В июне 2022 года бывший гендиректор «Сбербанк капитала» и экс-президент «Евроцемент груп» Ашот Хачатурянц стал совладельцем ряда предприятий «Алмаз групп». Хачатурянц теперь владеет 60% ООО «Алмаз тех» (основной вид деятельности — производство алюминия). Этому ООО, в свою очередь, принадлежит ключевой актив группы — ООО «Алмаз удобрения» (производитель минеральных удобрений).
- УПАКОВКА, МАРКИРОВКА, ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ
- Азот в природе
- Распространённость
- Биологическая роль
- Круговорот азота в природе
- Токсикология азота и его соединений
- ПРИЛОЖЕНИЕ 1 (рекомендуемое). ОПРЕДЕЛЕНИЕ ОБЪЕМНОЙ ДОЛИ ВОДЯНОГО ПАРА КОНДЕНСАЦИОННЫМ МЕТОДОМ
- Применение
- Жидкий азот
- ГАРАНТИИ ИЗГОТОВИТЕЛЯ
- История открытия
- ПРАВИЛА ПРИЕМКИ
- Происхождение названия
- Станции ТГА новогопоколения ставят рекорды энергоэффективности
- ТРЕБОВАНИЯ БЕЗОПАСНОСТИ
- Маркировка баллонов
- ПРИЛОЖЕНИЕ 2 (рекомендуемое). ОПРЕДЕЛЕНИЕ КОЛИЧЕСТВА АЗОТА, ОТПУСКАЕМОГО ПОТРЕБИТЕЛЮ
- Свойства
- Фазовая диаграмма
- Химические свойства, строение молекулы
- Промышленное связывание атмосферного азота
- Соединения азота
- Кемеровский «АЗОТ» повысит свою энергоэффективность с оборудовнием ЭНПРО.
- Опасность для здоровья
- Получение
- Нагревание дихромата калия с сульфатом аммония
- Разложение азидов
- Реакция воздуха с раскалённым коксом
- Перегонка воздуха
- Пропускание аммиака над оксидом меди (II)
- Энергоэффективные способы
УПАКОВКА, МАРКИРОВКА, ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ
Упаковка, маркировка, транспортирование и хранение газообразного и жидкого технического азота, азота повышенной чистоты и азота особой чистоты — по ГОСТ 26460-85, при этом номинальное давление азота при 20 °С в баллонах и автореципиентах (15,0±0,5) МПа (150±5) кгс/см2 или (20,0±1,0) МПа (200±10) кгс/см2.
(Измененная редакция, Изм. N 2, 3).
Азот в природе
Основная статья: Изотопы азота
Природный азот состоит из двух стабильных изотопов 14N — 99,635 % и 15N — 0,365 %.
Искусственно получены четырнадцать радиоактивных изотопов азота с массовыми числами от 10 до 13 и от 16 до 25. Все они являются очень короткоживущими изотопами. Самый стабильный из них 13N имеет период полураспада 10 мин.
Спин ядер стабильных изотопов азота: 14N — 1; 15N — 1/2.
Распространённость
Азот — один из самых распространённых элементов на Земле. Вне пределов Земли азот обнаружен в газовых туманностях, солнечной атмосфере, на Уране, Нептуне, в межзвёздном пространстве и др. Атмосферы таких планет-спутников как Титан, Тритон, а также карликовой планеты Плутон в основном состоят из азота. Азот — четвёртый по распространённости элемент Солнечной системы (после водорода, гелия и кислорода).
Азот в форме двухатомных молекул N2 составляет большую часть атмосферы Земли, где его содержание составляет 75,6 % (по массе) или 78,084 % (по объёму), то есть около 3,87⋅1015 т.
Содержание азота в земной коре, по данным разных авторов, составляет (0,7—1,5)⋅1015 т (причём в гумусе — порядка 6⋅1010 т), а в мантии Земли — 1,3⋅1016 т. Такое соотношение масс заставляет предположить, что главным источником азота служит верхняя часть мантии, откуда он поступает в другие оболочки Земли с извержениями вулканов.
Масса растворённого в гидросфере азота, учитывая, что одновременно происходят процессы растворения азота атмосферы в воде и выделения его в атмосферу, составляет около 2⋅1013 т, кроме того, примерно 7⋅1011 т азота содержатся в гидросфере в виде соединений.
Биологическая роль
Азот является химическим элементом, необходимым для существования животных и растений, он входит в состав белков (16—18 % по массе), аминокислот, нуклеиновых кислот, нуклеопротеидов, хлорофилла, гемоглобина и др. В составе живых клеток по числу атомов азота около 2 %, по массовой доле — около 2,5 % (четвёртое место после водорода, углерода и кислорода). В связи с этим значительное количество связанного азота содержится в живых организмах, «мёртвой органике» и дисперсном веществе морей и океанов. Это количество оценивается примерно в 1,9⋅1011 т. В результате процессов гниения и разложения азотсодержащей органики, при условии благоприятных факторов окружающей среды, могут образоваться природные залежи полезных ископаемых, содержащие азот, например, «чилийская селитра» (нитрат натрия с примесями других соединений), норвежская, индийская селитры.
Химия гидридов азота при давлениях порядка 800 ГПа (около 8 миллионов атмосфер) более разнообразна, чем химия углеводородов при нормальных условиях. Отсюда появилась гипотеза, что азот может быть основой пока неоткрытой жизни на таких планетах, как Уран и Нептун.
Круговорот азота в природе
Основная статья: Круговорот азота
Фиксация атмосферного азота в природе происходит по двум основным направлениям — абиогенному и биогенному. Первый путь включает главным образом реакции азота с кислородом. Так как азот химически весьма инертен, для окисления требуются большие количества энергии (высокие температуры). Эти условия достигаются при разрядах молний, когда температура достигает 25000 °C и более. При этом происходит образование различных оксидов азота. Существует также вероятность, что абиотическая фиксация происходит в результате фотокаталитических реакций на поверхности полупроводников или широкополосных диэлектриков (песок пустынь).
Однако основная часть молекулярного азота (около 1,4⋅108 т/год) фиксируется биотическим путём. Долгое время считалось, что связывать молекулярный азот могут только небольшое количество видов микроорганизмов (хотя и широко распространённых на поверхности Земли): бактерии Azotobacter и Clostridium, клубеньковые бактерии бобовых растений Rhizobium, цианобактерии Anabaena, Nostoc и др. Сейчас известно, что этой способностью обладают многие другие организмы в воде и почве, например, актиномицеты в клубеньках ольхи и других деревьев (всего 160 видов). Все они превращают молекулярный азот в соединения аммония (NH4+). Этот процесс требует значительных затрат энергии (для фиксации 1 г атмосферного азота бактерии в клубеньках бобовых расходуют порядка 167,5 кДж, то есть окисляют примерно 10 г глюкозы). Таким образом, видна взаимная польза от симбиоза растений и азотфиксирующих бактерий — первые предоставляют вторым «место для проживания» и снабжают полученным в результате фотосинтеза «топливом» — глюкозой, вторые обеспечивают необходимый растениям азот в усваиваемой ими форме.
Азот в форме аммиака и соединений аммония, получающийся в процессах биогенной азотфиксации, быстро окисляется до нитратов и нитритов (этот процесс носит название нитрификации). Последние, не связанные тканями растений (и далее по пищевой цепи травоядными и хищниками), недолго остаются в почве. Большинство нитратов и нитритов хорошо растворимы, поэтому они смываются водой и, в конце концов, попадают в мировой океан (этот поток оценивается в 2,5—8⋅107 т/год).
Азот, включённый в ткани растений и животных, после их гибели подвергается аммонификации (разложению содержащих азот сложных соединений с выделением аммиака и ионов аммония) и денитрификации, то есть выделению атомарного азота, а также его оксидов. Эти процессы целиком происходят благодаря деятельности микроорганизмов в аэробных и анаэробных условиях.
В отсутствие деятельности человека процессы связывания азота и нитрификации практически полностью уравновешены противоположными реакциями денитрификации. Часть азота поступает в атмосферу из мантии с извержениями вулканов, часть прочно фиксируется в почвах и глинистых минералах, кроме того, постоянно идёт утечка азота из верхних слоёв атмосферы в межпланетное пространство.
Токсикология азота и его соединений
Сам по себе атмосферный азот достаточно инертен, чтобы оказывать непосредственное влияние на организм человека и млекопитающих. Тем не менее, при повышенном давлении он вызывает наркоз, опьянение или удушье (при недостатке кислорода); при быстром снижении давления азот вызывает кессонную болезнь.
Многие соединения азота очень активны и нередко токсичны.
ПРИЛОЖЕНИЕ 1 (рекомендуемое). ОПРЕДЕЛЕНИЕ ОБЪЕМНОЙ ДОЛИ ВОДЯНОГО ПАРА КОНДЕНСАЦИОННЫМ МЕТОДОМ
Объемную долю водяного пара определяют приборами конденсационного типа с пороговой чувствительностью не выше 1,5 млн-1.
Относительная погрешность прибора не должна превышать 10%. Метод основан на измерении температуры насыщения газа водяным паром при появлении росы на охлажденной зеркальной поверхности.
Анализ проводят по инструкции, приложенной к прибору.
Объемную долю водяного пара в соответствии с найденной температурой насыщения определяют по таблице.
Объемная доля водяного пара, млн-1(ppm)Температура насыщения, °С2,55-703,44-684,60-666,10-648,07-6210,6-6014,0-5818,3-5623,4-5431,1-5239,4-5049,7-4863,2-4680-44101-42127-40
Примечание. Объемная доля, равная 1 млн-1, соответствует 1·10-4%.
Применение
Промышленное применение газообразного азота обусловлено его инертными свойствами. Газообразный азот пожаро- и взрывобезопасен, препятствует окислению, гниению. В нефтедобывающей промышленности газообразный азот применяется для обеспечения безопасного бурения, используется в процессе капитального и текущего ремонта скважин. Кроме того, газообразный азот высокого давления используют в газовых методах повышения нефтеотдачи пласта. В нефтехимии азот применяется для продувки резервуаров и трубопроводов, проверки работы трубопроводов под давлением, увеличения выработки месторождений. В горнодобывающем деле азот может использоваться для создания в шахтах взрывобезопасной среды, для распирания пластов породы, тушения эндогенных пожаров. В производстве электроники азот применяется для продувки областей, не допускающих наличия окисляющего кислорода. Если в процессе, традиционно проходящем с использованием воздуха, окисление или гниение являются негативными факторами — азот может успешно заместить воздух.
Газообразным азотом заполняют камеры шин шасси летательных аппаратов. Кроме того, в последнее время заполнение шин азотом стало популярно и среди автолюбителей, хотя однозначных доказательств эффективности использования азота вместо воздуха для наполнения автомобильных шин нет.
Жидкий азот

Слабокипящий жидкий азот в металлическом стакане
Жидкий азот применяется как хладагент и для криотерапии.
Важной областью применения азота является его использование для дальнейшего синтеза самых разнообразных соединений, содержащих азот, таких, как аммиак, азотные удобрения, взрывчатые вещества, красители и т. Более 3/4 промышленного азота идёт на синтез аммиака.
Большие количества азота используются в коксовом производстве («сухое тушение кокса») при выгрузке кокса из коксовых батарей, а также для «передавливания» топлива в ракетах из баков в насосы или двигатели.
В пищевой промышленности азот зарегистрирован в качестве пищевой добавки E941, как газовая среда для упаковки и хранения, хладагент, а жидкий азот применяется при разливе масел и негазированных напитков для создания избыточного давления и инертной среды в мягкой таре.
Жидкий азот нередко демонстрируется в кинофильмах в качестве вещества, способного мгновенно заморозить достаточно крупные объекты. Это широко распространённое заблуждение. Даже для замораживания цветка необходимо достаточно продолжительное время. Это связано отчасти с весьма низкой теплоёмкостью азота. По этой же причине весьма затруднительно охлаждать, скажем, замки до −196 °C и раскалывать их одним ударом.
Литр жидкого азота, испаряясь и нагреваясь до 20 °C, образует примерно 700 литров газа. По этой причине жидкий азот хранят в специальных сосудах Дьюара с вакуумной изоляцией открытого типа или криогенных ёмкостях под давлением. На этом же факте основан принцип тушения пожаров жидким азотом. Испаряясь, азот вытесняет кислород, необходимый для горения, и пожар прекращается. Так как азот, в отличие от воды, пены или порошка, просто испаряется и выветривается, азотное пожаротушение — самый эффективный с точки зрения сохранности ценностей механизм тушения пожаров.
Заморозка жидким азотом живых существ с возможностью последующей их разморозки проблематична. Проблема заключается в невозможности заморозить (и разморозить) существо достаточно быстро, чтобы неоднородность заморозки не сказалась на его жизненных функциях. Станислав Лем, фантазируя на эту тему в книге «Фиаско», придумал экстренную систему заморозки азотом, в которой шланг с азотом, выбивая зубы, вонзался в рот астронавта и внутрь его подавался обильный поток азота.
В качестве легирующей добавки к кремнию, образует высокопрочное соединение (керамику) нитрид кремния, обладающее высокой вязкостью и прочностью.
ГАРАНТИИ ИЗГОТОВИТЕЛЯ
Изготовитель гарантирует соответствие качества газообразного и жидкого азота требованиям настоящего стандарта при соблюдении условий хранения и транспортирования.
Гарантийный срок хранения газообразного азота — 18 мес со дня изготовления продукта.
История открытия
В 1772 году Генри Кавендиш провёл опыт: он многократно пропускал воздух над раскалённым углём, затем обрабатывал его щёлочью, в результате получался остаток, который Кавендиш назвал удушливым (или мефитическим) воздухом. С позиций современной химии ясно, что в реакции с раскалённым углём кислород воздуха связывался в углекислый газ, который затем поглощался щёлочью. При этом остаток газа представлял собой по большей части азот. Таким образом, Кавендиш выделил азот, но не сумел понять, что это новое простое вещество (химический элемент), и описал его как мефитический воздух (от английского mephitic — ‘вредный’). В том же году Кавендиш сообщил об этом опыте Джозефу Пристли.
Интересен тот факт, что он сумел связать азот с кислородом при помощи разрядов электрического тока, а после поглощения оксидов азота в остатке получил небольшое количество газа, абсолютно инертного, хотя, как и в случае с азотом, не смог понять, что выделил новый химический элемент — инертный газ аргон.
Джозеф Пристли в это время проводил серию экспериментов, в которых также связывал кислород воздуха и удалял полученный углекислый газ, то есть также получал азот, однако, будучи сторонником господствующей в те времена теории флогистона, также неверно истолковал полученные результаты — он решил, что выделил флогистированный воздух (т. насыщенный флогистоном).
В сентябре 1772 года шотландский химик Даниэль Резерфорд опубликовал магистерскую диссертацию «О так называемом фиксируемом и мефитическом воздухе», в которой описал азот как вредный, ядовитый воздух и предположил, что это новый химический элемент, а также описал основные свойства азота (не реагирует со щелочами, не поддерживает горения, непригоден для дыхания). Резерфорд также был сторонником флогистонной теории, поэтому также не смог понять, что же он выделил. Таким образом, чётко определить первооткрывателя азота невозможно.
В то же время азот выделил Карл Шееле: летом 1772 года он получил азот по методу Кавендиша и исследовал его в течение пяти лет, затем опубликовал результаты своих исследований. В этой публикации Шееле первым описал воздух как смесь отдельных газов: «огненного воздуха» (кислорода) и «грязного воздуха» (азота). Из-за того, что Шееле задержался с публикацией своих исследований, до сих пор идут споры о первооткрывателе азота.
ПРАВИЛА ПРИЕМКИ
Газообразный и жидкий азот принимают партиями. Партией считают однородный по своим качественным показателям азот одной сменной выработки, сопровождаемый одним документом о качестве, при этом при перевозке азота в цистернах или автореципиентах за партию принимают каждую цистерну или автореципиент.
Партией газообразного азота, транспортируемого по трубопроводу, считают любое количество азота, направляемого потребителю в течение 24 ч.
Каждая партия газообразного и жидкого азота должна сопровождаться документом о качестве, содержащим следующие данные:
наименование предприятия-изготовителя и его товарный знак;
наименование и сорт продукта;
объем газообразного азота в кубических метрах, массу жидкого азота в тоннах или килограммах (вычисленные в соответствии с приложением 2);
результаты проведенных анализов или подтверждение о соответствии продукта требованиям настоящего стандарта;
обозначение настоящего стандарта;
номер цистерны жидкого азота.
(Измененная редакция, Изм. N 2).
Для проверки изготовителем качества газообразного азота, транспортируемого в баллонах, отбирают 2% баллонов от партии до 200 баллонов и пять баллонов от партии более 200 баллонов.
Для проверки изготовителем качества жидкого азота пробу отбирают от каждой транспортной цистерны номинальной вместимостью 10 м и более. При наполнении цистерн меньшей вместимостью или сосудов Дьюара пробу отбирают из стационарной емкости до наполнения партии или из разделительного аппарата до и после наполнения партии.
Объем пробы жидкого азота не должен быть менее 2,5 дм3.
Для проверки потребителем качества газообразного азота отбирают 2% баллонов от партии, но не менее двух баллонов при партии менее 100 баллонов.
Для проверки потребителем качества жидкого азота пробу отбирают от каждой транспортной цистерны или 10% единиц продукции.
Для проверки изготовителем и потребителем качества газообразного азота, транспортируемого в автореципиентах, пробу отбирают от каждого автореципиента.
Для проверки изготовителем и потребителем качества газообразного азота, транспортируемого по трубопроводу, пробу отбирают не менее одного раза за 24 ч.
При получении неудовлетворительных результатов анализа газообразного или жидкого азота хотя бы по одному из показателей должна проводиться повторная проверка на удвоенной выборке или удвоенном объеме проб от той же партии.
Результаты повторных анализов распространяются на всю партию.
Происхождение названия
Название «азо́т» (фр. azote, по наиболее распространённой версии, от др. -греч. ἄζωτος — безжизненный), вместо предыдущих названий («флогистированный», «мефитический» и «испорченный» воздух) предложил в 1787 году Антуан Лавуазье, который в то время в составе группы других французских учёных разрабатывал принципы химической номенклатуры, в том же году это предложение опубликовано в труде «Метод химической номенклатуры. Как показано выше, в то время уже было известно, что азот не поддерживает ни горения, ни дыхания. Это свойство и сочли наиболее важным. Хотя впоследствии выяснилось, что азот, наоборот, крайне необходим для всех живых существ, название сохранилось во французском и русском языках. Окончательно в русском языке этот вариант названия закрепился после выхода в свет книги Германа Гесса «Основания чистой химии» в 1831 году.
Само слово «азот» (без связи с газом) известно с древности и употреблялось философами и алхимиками средневековья для обозначения «первичной материи металлов», так называемого «меркурия» у философов, «двойного меркурия» у алхимиков. «Первичную материю металлов» алхимики считали «альфой и омегой» всего сущего. И слово для её обозначения составили из начальных и конечных букв алфавитов трёх языков, считавшихся священными, — латинского, греческого и древнееврейского: а, альфа, алеф и зет, омега, тов — AAAZOT. Инициатор создания новой химической номенклатуры Гитон де Морво отмечал в своей «Методической энциклопедии» (1786 год) алхимическое значение термина.
Многие современники Лавуазье считали название элемента неудачным, в частности, Жан-Антуан Шапталь предложил название фр. nitrogène — «рождающий селитру» (и использовал это название в своей книге «Элементы химии»). Поныне соединения азота называют «нитраты», «нитриты» и «нитриды».
Во французском языке название «нитроген» не прижилось, зато в английском, испанском, венгерском и норвежском используется производное от этого слова. В немецком языке используется название нем. Stickstoff, что означает «удушающее вещество», аналогично в нидерландском; схожие по значению названия используются в некоторых славянских языках, например, хорватское и словенское dušik (пр. «душик»).
Название «азот», помимо французского и русского, принято в итальянском, турецком и ряде славянских языков, а также во многих языках народов бывшего СССР.
До принятия символа N в России, Франции и других странах использовался символ Az, который можно видеть, например, в статье А. Бутлерова об аминах 1864 года.
Станции ТГА новогопоколения ставят рекорды энергоэффективности
Азотные мембранные станции серии ТГА вырабатывают азот из атмосферного воздуха непосредственно на месте эксплуатации и сразу подают его на объект под высоким давлением. Наиболее популярная модель передвижной азотной компрессорной станции этой серии – ТГА-10/251 С95 производства Краснодарского Компрессорного Завода. Компрессорная установка надежно обеспечивает следующие характеристики по азоту:
• давление нагнетания – 250 атмосфер;• производительность – 10 нм3/мин. ;• концентрация – 95 %.
Станции с такими характеристиками наилучшим образом подходят для эксплуатации на объектах нефтегазовой и угольной промышленности, трубопроводного транспорта.
Новое поколение передвижной азотной станции ТГА-10/251 С95, запущенное в производство в 2020 году, становится еще привлекательней для заказчиков за счет:
• повышения энергоэффективности,• улучшения массогабаритных характеристик,• нового уровня эргономичности и ремонтопригодности,• повышения мобильности при транспортировке,• экономичности.
Какие же инновационные решения позволили добиться существенных улучшений?В первую очередь – это использование в станции нового компрессорного агрегата – усовершенствованного двухрядного поршневого пятиступенчатого оппозитного компрессора модели 2ГМ2,5-10/251М. Ранее в азотных станциях с аналогичными характеристиками устанавливался четырехрядный шестиступенчатый компрессор 4ГМ2,5-10/251, поскольку более компактная и экономичная двухрядная модель не позволяла добиться получения концентрации азота на выходе более 90% при сохранении производительности 10 нм3/мин. Теперь благодаря применению нового высокоэнергоэффективного двухрядного компрессорного агрегата впервые удалось достичь и надежно поддерживать уровень концентрации азота 95%, подавая его поддавлением 250 атмосфер со стабильной производительностью 10 нм3/мин. при использовании более легкого и компактного двухрядного компрессора.
Какие изменения в конструкции нового двухрядного компрессора помогли вывести его на более высокий уровень производительности и энергоэффективности? Наибольшее количество инновационных решений внедрено в основной рабочий орган компрессора – его цилиндро-поршневую группу (ЦПГ). Глубокая модернизация ЦПГ с применением в ее конструкции ряда изобретений, оптимизация параметров за счет изменения соотношений диаметров ступеней компрессора, усовершенствование конфигурации других элементов группы, применение новых инновационных материалов для изготовления узлов и деталей, использование легкосплавных поршней – все это позволило добиться надежного обеспечения параметров, недостижимых ранее.
Инновациями в цилиндро-поршневую группу компрессора список новшеств не ограничивается. Дополнительно за счет применения обновленной конструкции и использования новых высокопрочных и износостойких материалов был усилен коленвал, теперь способный воспринимать более высокие нагрузки, недопустимые для предыдущей модели.
Какие преимущества получает заказчик, приобретая именно новое поколение азотной станции ТГА-10/251 С95, посравнению с предыдущим?Благодаря применению нового двухрядного компрессора вместо четырехрядного существенно снижаются масса и габариты компрессорного агрегата и всей компрессорной станции. Если четырехрядный компрессор, используемый ранее, весил 4580 кг, то современный двухрядный, используемый в новом поколении станции, – всего 2880 кг. Также значительно уменьшены и габариты компрессорного агрегата. Это позволило впервые установить новую азотную станцию этой модели на облегченное более маневренное и экономичное трехосное шасси КамАЗ-43118, а не на массивное четырехосное шасси КамАЗ-63501, как это делалось ранее. В результате общий вес станции снизился на 7600 кг, с 26500 кг для предыдущего поколения до 18900 кг для нового поколения самоходной азотной станции.
Оптимизация и упрощение конструкции компрессорного агрегата, сокращение количества рядов компрессора с четырех до двух, а ступеней сжатия — с шести до пяти позволили ощутимо снизить расход топлива и повысить энергоэффективность азотной станции в целом как в рабочем режиме, так и при транспортировке к местам эксплуатации. Улучшена эргономичность, снижен уровень шума при работе компрессорногоагрегата. Эксплуатировать станцию стало легче и удобнее, сокращено количество параметров, за которыми должен следить машинист, обновлена система автоматического управления и сигнализации.
Благодаря уменьшению количества узлов и механизмов самого компрессорного агрегата, оптимизации и более компактной компоновке, сокращению по габаритам теплообменного оборудования газоохладительной системы компрессора освободилось пространство внутри станции, открылся свободный доступ для технического обслуживания и ремонта. Повысился уровень ремонтопригодности, а обслуживание и ремонт азотной станции стали более удобными и менее затратными.
Снижение массы азотной станции и установка на более маневренное облегченное трехосное шасси КамАЗ-43118делают удобными транспортировку станции по дорогам общего пользования, ее позиционирование и установку в рабочее положение непосредственно на объекте эксплуатации при ограниченных условиях для маневрирования. В целом, новое поколение азотной станции ТГА-10/251 С95 с двухрядным поршневым пятиступенчатым оппозитным компрессором модели 2ГМ2,5-10/251М стало более экономичным в эксплуатации и при транспортировке, в техническом обслуживании и при ремонте.
Наличие собственного конструкторского бюро и система оперативного внедрения запатентованных инновационных решений в производство позволяют Краснодарскому Компрессорному Заводу разрабатывать, производить и предлагать заказчикам самые передовые модели азотных станций. Азотные станции серии ТГА являются лауреатами конкурса «Сто лучших товаров России», обладателями золотого знака, они отмечены специальной наградой – кубком, вручаемым победителям «За успехи в импортозамещении». Азотная станция модели ТГА-10/251 С95 наиболее востребована в нефтегазовой и угольной промышленности для решения следующих задач:• Повышение нефтеотдачи пласта при добыче нефти;• Обеспечение работ при капитальном и текущем ремонте скважин;• Консервация и расконсервация скважин;• Обеспечение безопасного бурения;• Испытания / опрессовка газо- и нефтепроводов;• Азотирование / инертизация газо- и нефтепроводов;• Очистка газо- и нефтепроводов;• Азотирование / инертизация емкостей;• Профилактика эндогенных пожаров в угольных шахтах;• Азотное пожаротушение.
Надежность и эффективность азотных компрессорных станций серии ТГА проверены временем. Клиенты эксплуатируют станции ТГА в течение десяти и более лет и продолжают заказывать азотные установки именно этой серии. Постоянные заказчики Краснодарского Компрессорного Завода уже ждут азотные компрессорные станции модели ТГА-10/251 С95 нового поколения и связывают повышение эффективности эксплуатации парка компрессорного оборудования с приобретением нового поколения станции.
ТРЕБОВАНИЯ БЕЗОПАСНОСТИ
Азот нетоксичен, невзрывоопасен.
Накопление газообразного азота вызывает явление кислородной недостаточности и удушья. Содержание кислорода в воздухе рабочей зоны должно быть не менее 19% (по объему).
Жидкий азот — низкокипящая жидкость, которая может вызвать обмораживание кожи и поражение слизистой оболочки глаз. При отборе проб жидкого азота необходимо работать в защитных очках.
При повышении в жидком азоте содержания кислорода до 30% (по объему) (например, в результате испарения жидкого азота) возможно образование пожаро-, взрывоопасных смесей с органическими веществами. Поэтому в ваннах или других открытых сосудах, предназначенных для проведения работ в среде жидкого азота, присутствие масел, органических растворителей и других пожаро-, взрывоопасных веществ недопустимо.
Перед использованием и проведением работ с применением жидкого азота должна проводиться проверка содержания в нем кислорода.
Слив жидкого азота должен проводиться в специально отведенных местах, не имеющих покрытий из асфальта, дерева или других органических материалов.
Перед проведением ремонтных работ или освидетельствованием бывшей в эксплуатации транспортной или стационарной емкости жидкого азота ее необходимо отогреть до температуры окружающей среды и продуть воздухом.
Начинать работать разрешается только после того, как содержание кислорода внутри цистерны и оборудования будет не менее 19% (по объему).
При работе в атмосфере азота необходимо пользоваться изолирующим кислородным прибором или шланговым противогазом.
Маркировка баллонов
Основная статья: Окраска и маркировка баллонов с газами
Выпущенные в России баллоны с азотом, согласно требованиям ПБ 03-576-03, должны быть окрашены в чёрный цвет с коричневой полосой и надписью жёлтого цвета. ГОСТ 26460-85 не требует полосы, но надпись должна содержать сведения о чистоте азота (особой чистоты, высокой чистоты, повышенной чистоты).
ПРИЛОЖЕНИЕ 2 (рекомендуемое). ОПРЕДЕЛЕНИЕ КОЛИЧЕСТВА АЗОТА, ОТПУСКАЕМОГО ПОТРЕБИТЕЛЮ
Объем газообразного азота в стальном баллоне (Vп) в м3 при 20 °С и 101,3 кПа вычисляют по формулегде Vб — вместимость баллона, дм3. В расчетах принимается среднестатистическая величина вместимости баллонов не менее чем из 100 шт
K — коэффициент для вычисления объема газа в баллоне, учитывающий сжимаемость азота, давление и температуру газа в баллоне, вычисляют по формуле
где P — давление газа в баллоне, измеренное манометром, кгс/см2;
0,968 — коэффициент пересчета технических атмосфер (кгс/см2) в физические атмосферы;
t — температура газа в баллоне при измерении давления, °С;
Z — коэффициент сжимаемости азота при температуре t°С, указанный в таблице.
Давление, МПа, (кгс/см2)Температура, °С-50-250202550Коэффициент сжимаемости азота10 (100)0,9050,9180,9851,0011,0051,01814,5 (145)0,930,951,0011,021,0231,03720,4 (200)0,9580,9681,0351,0531,061,076
Например, при поставке газообразного азота в баллонах по ГОСТ 949-73 вместимостью 40 дм3 количество газа в баллоне при рабочем давлении 150 кгс/см2 при 20 °С составляет м.
Количество жидкого азота, отпускаемого потребителю в транспортных цистернах, определяют по указателю уровня жидкого азота (УЖА) в тоннах.
При переводе массы жидкого азота в м3 газообразного азота при 20 °С и 101,3 кПа пользуются формулой где m — масса жидкого азота, т; 1,165 — плотность газообразного азота, кг/м3.
Свойства

Оптический эмиссионный спектр азота
При нормальных условиях азот — это бесцветный газ, не имеет запаха, мало растворим в воде (2,3 мл/100 г при 0 °C, 1,5 мл/100 г при 20 °C, 1,1 мл/100 г при 40 °C, 0,5 мл/100 г при 80 °C), плотность 1,2506 кг/м³ (при н.
В жидком состоянии (темп. кипения -195,8 °C) — бесцветная, подвижная, как вода, жидкость. Плотность жидкого азота 808 кг/м³. При контакте с воздухом поглощает из него кислород.
При -209,86 °C азот переходит в твёрдое состояние в виде снегоподобной массы или больших белоснежных кристаллов. При контакте с воздухом поглощает из него кислород, при этом плавится, образуя раствор кислорода в азоте.
Известны три кристаллические модификации твёрдого азота. В интервале 36,61 — 63,29 К существует фаза β-N2 с гексагональной плотной упаковкой, пространственная группа P63/mmc, параметры решётки a=3,93 Å и c=6,50 Å. При температуре ниже 36,61 К устойчива фаза α-N2 с кубической решёткой, имеющая пространственную группу Pa3 или P213 и период a=5,660 Å. Под давлением более 3500 атмосфер и температуре ниже 83 K образуется гексагональная фаза γ-N2.
Фазовая диаграмма
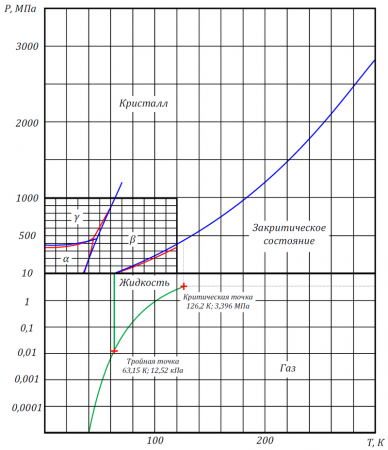
Фазовая диаграмма азота показана на рисунке.
Химические свойства, строение молекулы
Азот в свободном состоянии существует в форме двухатомных молекул N2, электронная конфигурация которых описывается формулой σs²σs*2πx, y4σz², что соответствует тройной связи между атомами азота N≡N (длина связи dN≡N = 0,1095 нм). Вследствие этого молекула азота крайне прочна, для реакции диссоциации N2 ↔ 2 N изменение энтальпии в реакции ΔH°298 = 945 кДж/моль, константа скорости реакции К298 = 10−120, то есть диссоциация молекул азота при нормальных условиях практически не происходит (равновесие практически полностью сдвинуто влево). Молекула азота неполярна и слабо поляризуется, силы взаимодействия между молекулами очень слабые, поэтому в обычных условиях азот газообразен.
Даже при 3000 °C степень термической диссоциации N2 составляет всего 0,1 %, и лишь при температуре около 5000 °C достигает нескольких процентов (при нормальном давлении). В высоких слоях атмосферы происходит фотохимическая диссоциация молекул N2. В лабораторных условиях можно получить атомарный азот, пропуская газообразный N2 при сильном разрежении через поле высокочастотного электрического разряда. Атомарный азот намного активнее молекулярного: в частности, при обычной температуре он реагирует с серой, фосфором, мышьяком и с рядом металлов, например, со ртутью.
Вследствие большой прочности молекулы азота некоторые его соединения эндотермичны (многие галогениды, азиды, оксиды), то есть энтальпия их образования положительна, а соединения азота термически малоустойчивы и довольно легко разлагаются при нагревании. Именно поэтому азот на Земле находится по большей части в свободном состоянии.
Ввиду своей значительной инертности азот при обычных условиях реагирует только с литием:
6Li + N2 ⟶ 2Li3N
при нагревании он реагирует с некоторыми другими металлами и неметаллами, также образуя нитриды:
3Mg + N2 ⟶ Mg3N2
2B + N2 ⟶ 2BN
Наибольшее практическое значение имеет нитрид водорода (аммиак) NH3, получаемый взаимодействием водорода с азотом (см. ниже).
В электрическом разряде реагирует с кислородом, образуя оксид азота (II) NO.
Описано несколько десятков комплексов с молекулярным азотом.
Промышленное связывание атмосферного азота
Соединения азота чрезвычайно широко используются в химии, невозможно даже перечислить все области, где находят применение вещества, содержащие азот: это индустрия удобрений, взрывчатых веществ, красителей, медикаментов и проч. Хотя колоссальные количества азота доступны в прямом смысле слова «из воздуха», из-за описанной выше прочности молекулы азота N2 долгое время оставалась нерешённой задача получения соединений, содержащих азот, из воздуха; большая часть соединений азота добывалась из его минералов, таких, как чилийская селитра. Однако сокращение запасов этих полезных ископаемых, а также рост потребности в соединениях азота заставил форсировать работы по промышленному связыванию атмосферного азота.
Наиболее распространён аммиачный способ связывания атмосферного азота. Обратимая реакция синтеза аммиака:
N2 + 3H2 ⟷ 2NH3
экзотермическая (тепловой эффект 92 кДж) и идёт с уменьшением объёма, поэтому для сдвига равновесия вправо в соответствии с принципом Ле Шателье — Брауна необходимо охлаждение смеси и высокие давления. Однако с кинетической точки зрения снижение температуры невыгодно, так как при этом сильно снижается скорость реакции — уже при 700 °C скорость реакции слишком мала для её практического использования.
В таких случаях используется катализ, так как подходящий катализатор позволяет увеличить скорость реакции без сдвига равновесия. В процессе поиска подходящего катализатора было испробовано около двадцати тысяч различных соединений. По совокупности свойств (каталитическая активность, стойкость к отравлению, дешевизна) наибольшее применение получил катализатор на основе металлического железа с примесями оксидов алюминия и калия. Процесс ведут при температуре 400—600 °C и давлениях 10—1000 атмосфер.
Следует отметить, что при давлениях выше 2000 атмосфер синтез аммиака из смеси водорода и азота идёт с высокой скоростью и без катализатора. Например, при 850 °C и 4500 атмосфер выход продукта составляет 97 %.
Существует и ещё один, менее распространённый способ промышленного связывания атмосферного азота — цианамидный метод, основанный на реакции карбида кальция с азотом при 1000 °C. Реакция происходит по уравнению:
CaC2 + N2 ⟶ CaCN2 + C
Реакция экзотермична, её тепловой эффект 293 кДж.
Ежегодно из атмосферы Земли промышленным путём отбирается примерно 1⋅106 т азота.
Соединения азота
Степени окисления азота в соединениях −3, −2, −1, 0, +1, +2, +3, +4, +5.
- Соединения азота в степени окисления −3 представлены нитридами, из которых практически наиболее важен аммиак;
- Соединения азота в степени окисления −2 менее характерны, представлены пернитридами, из которых самый важный пернитрид водорода N2H4, или гидразин (существует также крайне неустойчивый пернитрид водорода N2H2, диимид);
- Соединения азота в степени окисления −1: NH2OH (гидроксиламин) — неустойчивое основание, применяющееся, наряду с солями гидроксиламмония, в органическом синтезе;
- Соединения азота в степени окисления +1: оксид азота (I) N2O (закись азота, веселящий газ), азотноватистая кислота;
- Соединения азота в степени окисления +2: оксид азота (II) NO (монооксид азота), азотноватая кислота;
- Соединения азота в степени окисления +3: оксид азота (III) N2O3 (сесквиоксид азота, триоксид диазота), азотистая кислота, производные аниона NO2−, трифторид азота (NF3);
- Соединения азота в степени окисления +4: оксид азота (IV) NO2 (диоксид азота, бурый газ);
- Соединения азота в степени окисления +5: оксид азота (V) N2O5 (пентаоксид диазота), азотная кислота, её соли — нитраты и другие производные, а также тетрафтораммоний NF4+ и его соли.
Кемеровский «АЗОТ» повысит свою энергоэффективность с оборудовнием ЭНПРО.
Для контроля потребления норм электрической энергии отдельными цехами и предприятием в целом, выявления непроизводственных затрат и прогнозирования диспетчерского графика на предприятиях Кемеровский «АЗОТ» началось внедрение Системы учёта и Системы диспетчерского контроля. Предложенное компанией ЭНПРО решение базируется на измерительных преобразователях SATEC, контроллерах ICP DAS и информационно-аналитическом программном комплексе SEDMAX. Данные по учёту и телемеханике будут передаваться на верхний уровень и с помощью SEDMAX обрабатываться, анализироваться и предоставляться в соответствующие службы предприятия и в смежные системы. В рамках проекта будут автоматизированы распределительные устройства КАО «АЗОТ» с классом напряжения от 0,4 до 220 кВ. Система учёта охватит 289 точек, а Система контроля состояния электрооборудования будет обрабатывать около 1100 сигналов. Кроме того, проектом предусмотрена модернизация диспетчерского пункта и создание диспетчерского щита на основе видеостены из LCD панелей. Новая система будет контролировать потребление электроэнергии и предоставлять данные для принятия решений:- по оптимизации процессов нормирования, планирования, оценки энергоэффективности внедряемых мероприятий,- по повышению энергоэффективности, по энергосбережению, и выявлению и реализации резервов экономии.
Опасность для здоровья
В обычных условиях азот не токсичен, однако при повышенном атмосферном давлении способен вызывать азотное отравление. Большинство соединений азота представляют сильную опасность для здоровья.
Азот относится ко 2-му классу опасности. Рейтинг NFPA 704: Опасность для здоровья: 3, огнеопасность: 0, реакционная способность: 0.
Периодическая система химических элементов Д. Менделеева1234567891011121314151617181HHe2LiBeBCNOFNe3NaMgAlSiPSClAr4KCaScTiVCrMnFeCoNiCuZnGaGeAsSeBrKr5RbSrYZrNbMoTcRuRhPdAgCdInSnSbTeIXe6CsBaLaCePrNdPmSmEuGdTbDyHoErTmYbLuHfTaWReOsIrPtAuHgTlPbBiPoAtRn7FrRaAcThPaUNpPuAmCmBkCfEsFmMdNoLrRfDbSgBhHsMtDsRgCnNhFlMcLvTsOg8UueUbnUbuUbbUbtUbqUbpUbhUbs
Получение
В лабораториях его можно получать по реакции разложения нитрита аммония:
NH4NO2 ⟶ N2↑ + 2H2O
Реакция экзотермическая, идёт с выделением 80 ккал (335 кДж), поэтому требуется охлаждение сосуда при её протекании (хотя для начала реакции требуется нагревание нитрита аммония).
Практически эту реакцию выполняют, добавляя по каплям насыщенный раствор нитрита натрия в нагретый насыщенный раствор сульфата аммония, при этом образующийся в результате обменной реакции нитрит аммония мгновенно разлагается.
Выделяющийся при этом газ загрязнён аммиаком, оксидом азота (I) и кислородом, от которых его очищают, последовательно пропуская через растворы серной кислоты, сульфата железа (II) и над раскалённой медью. Затем азот осушают.
Нагревание дихромата калия с сульфатом аммония
Ещё один лабораторный способ получения азота — нагревание смеси дихромата калия и сульфата аммония (в соотношении 2:1 по массе). Реакция идёт по уравнениям:
K2Cr2O7 + (NH4)2SO4 ⟶ (NH4)2Cr2O7 + K2SO4
(NH4)2Cr2O7 ⟶ N2↑ + Cr2O3 + 4H2O
Разложение азидов
Наиболее чистый азот можно получить разложением азидов металлов:
Реакция воздуха с раскалённым коксом
Так называемый «воздушный», или «атмосферный» азот, то есть смесь азота с благородными газами, получают путём реакции воздуха с раскалённым коксом, при этом образуется так называемый «генераторный», или «воздушный», газ — сырьё для химических синтезов и топливо. При необходимости из него можно выделить азот, поглотив монооксид углерода.
Перегонка воздуха
Молекулярный азот в промышленности получают фракционной перегонкой жидкого воздуха. Этим методом можно получить и «атмосферный азот». Также широко применяются азотные установки и станции, в которых используется метод адсорбционного и мембранного газоразделения.
Пропускание аммиака над оксидом меди (II)
Один из лабораторных способов — пропускание аммиака над оксидом меди (II) при температуре ~700 °C:
3CuO + 2NH3 ⟶ N2↑ + 3Cu + 3H2O
Аммиак берут из его насыщенного раствора при нагревании. Количество CuO в 2 раза больше расчётного. Непосредственно перед применением азот очищают от примеси кислорода и аммиака пропусканием над медью и её оксидом (II) (тоже ~700 °C), затем сушат концентрированной серной кислотой и сухой щёлочью. Процесс происходит довольно медленно, но он того стоит: газ получается весьма чистый.
Энергоэффективные способы
Антропогенное производство химически активных соединений азота в большой мере нарушает природный азотный цикл, следствием чего являются ряд проблем, связанных с ухудшением состояния природной среды и здоровья населения:
- токсичность аммиака по отношению к водной флоре и фауне,
- недостаток кислорода,
- эвтрофикация водоемов, приводящая, в частности, к возникновению мертвых зон в прибрежных областях морей и океанов,
- увеличение содержания в атмосфере оксида азота N₂O, относящегося к парниковым газам,
- снижение содержания озона в стратосфере и прямое воздействие на здоровье людей (например, метгемоглобинемия, вызываемая нитратами).
К наиболее распространенным способам биологического удаления азота из сточных вод относится нитри-денитрификация, являющаяся энергоемким процессом, предусматривающим высокий расход кислорода при аэрации, составляющей основную статью энегозатрат (до 50%). В этой связи с практикой очистки сточных вод от азота непосредственно связана энергоэффективность очистных сооружений.
К перспективной стратегии снижения энергозатрат относится раздельное удаление органических соединений углерода и соединений азота, обеспечивающее удаление биогенов и использование соединений углерода в качестве энергетического источника. В общем рассматривают три подхода к обращению со сточными водами с учетом содержащегося в них азота:
Автор статьи: Кофман Владимир Яковлевич








